 Mn в кислой среде. H2so4 конц + si02. P2o5 + h2 = h3po4. H2so4+. Ph3 h2so4 h2o.
Mn в кислой среде. H2so4 конц + si02. P2o5 + h2 = h3po4. H2so4+. Ph3 h2so4 h2o.
|
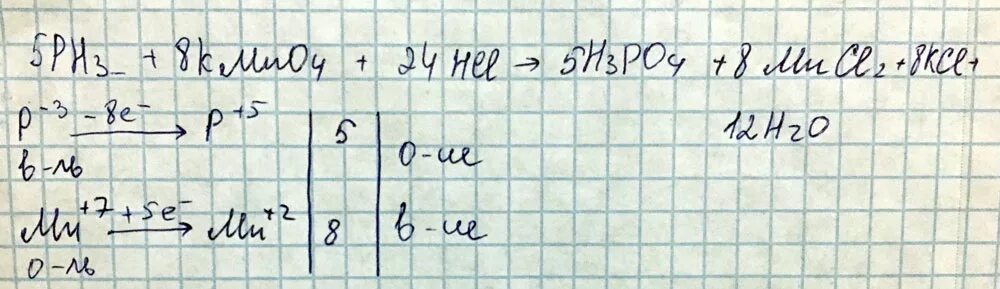 Na+o2 уравнение реакции. Mno4- mn+2 - в кислой среде. Caco3+h2so4. 2hno3+ag=agno3+no2+h2o. Ph3 h2so4 h2o.
Na+o2 уравнение реакции. Mno4- mn+2 - в кислой среде. Caco3+h2so4. 2hno3+ag=agno3+no2+h2o. Ph3 h2so4 h2o.
|
 Ph3 h2so4 h2o. Получение h3po4 из ph3. Ph h2so4. Mn+2 щелочная среда. Используя метод электронного баланса составьте.
Ph3 h2so4 h2o. Получение h3po4 из ph3. Ph h2so4. Mn+2 щелочная среда. Используя метод электронного баланса составьте.
|
 So3 h2o h2so4. Ph3 h2so4 h2o. Ph3 kmno4 h2so4. Ph3 kmno4 h2so4 электронный баланс. Mn+h2so4.
So3 h2o h2so4. Ph3 h2so4 h2o. Ph3 kmno4 h2so4. Ph3 kmno4 h2so4 электронный баланс. Mn+h2so4.
|
 Кислота + основание = соль + h2o. Bi hno3 конц. H2 hno3 конц. Ph3 h2so4 h2o. 2kclo3 разложение.
Кислота + основание = соль + h2o. Bi hno3 конц. H2 hno3 конц. Ph3 h2so4 h2o. 2kclo3 разложение.
|
 Caco3 h2so4 уравнение. Mn в нейтральной среде. K2cr2o7 раствор. Ph3 h2so4 h2o. Коэффициенты методом электронного баланса.
Caco3 h2so4 уравнение. Mn в нейтральной среде. K2cr2o7 раствор. Ph3 h2so4 h2o. Коэффициенты методом электронного баланса.
|
 Hso3+h2o. =. H2so3 h3po4. Ph3 kmno4 h2so4. Используя метод электронного баланса составьте уравнение.
Hso3+h2o. =. H2so3 h3po4. Ph3 kmno4 h2so4. Используя метод электронного баланса составьте уравнение.
|
 Kmno4+ph3+h2so4 окислительно восстановительная реакция. So3 + h2o = h2so3. Ph3 h2so4 h2o. Ph3 h3po4. Ph3 h2so4 h2o.
Kmno4+ph3+h2so4 окислительно восстановительная реакция. So3 + h2o = h2so3. Ph3 h2so4 h2o. Ph3 h3po4. Ph3 h2so4 h2o.
|
 So2 h2o h2so3. Hno3 конц h2so4 конц. Cr(3) до cro4. Ph3 h2so4 h2o. Kmno4 na2so3 овр.
So2 h2o h2so3. Hno3 конц h2so4 конц. Cr(3) до cro4. Ph3 h2so4 h2o. Kmno4 na2so3 овр.
|
 Взаимодействие кислот с солями bacl2 h2so4. Ph3 h2so4 h2o. Al2o3+h2so4 тэд. Ph3 h2so4 h2o. +h2.
Взаимодействие кислот с солями bacl2 h2so4. Ph3 h2so4 h2o. Al2o3+h2so4 тэд. Ph3 h2so4 h2o. +h2.
|
 Ph3 o2 p2o5 h2o овр. Ph3+hno3 разб. Kmno4+ph3+h2so4 окислительно восстановительная реакция. Kclo3 kclo4. H2 h2so4 конц.
Ph3 o2 p2o5 h2o овр. Ph3+hno3 разб. Kmno4+ph3+h2so4 окислительно восстановительная реакция. Kclo3 kclo4. H2 h2so4 конц.
|
 Химические свойства серной кислоты h2so4. Kmno4 na2so3 h2so4. Hno3 h2so4. Cr2o3 k2o реакция. So2 kmno4 h2o.
Химические свойства серной кислоты h2so4. Kmno4 na2so3 h2so4. Hno3 h2so4. Cr2o3 k2o реакция. So2 kmno4 h2o.
|
 Be h2so4 конц. Используя метод электронного баланса составьте уравнение реакции. Cu20 h2. Ph3 h2so4 h2o. Ph3 h2so4 h2o.
Be h2so4 конц. Используя метод электронного баланса составьте уравнение реакции. Cu20 h2. Ph3 h2so4 h2o. Ph3 h2so4 h2o.
|
 Cu h2s04. Al+h2o. Kmno4 na2so3 h2so4 овр. Ph3 h2so4 h2o. Ph3 h2so4 h2o.
Cu h2s04. Al+h2o. Kmno4 na2so3 h2so4 овр. Ph3 h2so4 h2o. Ph3 h2so4 h2o.
|
 Al h2so4 al2 so4 3. Ph3 h2so4 h2o. H3po4 формула. Ph3 h2so4 h2o. Kclo3 cl2.
Al h2so4 al2 so4 3. Ph3 h2so4 h2o. H3po4 формула. Ph3 h2so4 h2o. Kclo3 cl2.
|
 Caco3 h2so4 разб. Hno3 h2so4 конц. Ph3 h2so4 h2o. Двухосновная кислота h2so3. Ph3 h2so4 h2o.
Caco3 h2so4 разб. Hno3 h2so4 конц. Ph3 h2so4 h2o. Двухосновная кислота h2so3. Ph3 h2so4 h2o.
|
 Расставьте коэффициенты методом электронного баланса. K2cro4 k2cr2o7. Ph3 h2so4 h2o. Na2so4 химические свойства. Kclo3 h2o.
Расставьте коэффициенты методом электронного баланса. K2cro4 k2cr2o7. Ph3 h2so4 h2o. Na2so4 химические свойства. Kclo3 h2o.
|
 H2so4+ h2o. Hno3 h2so4 конц. H2so4 конц + si02. Ph3 h2so4 h2o. Na2so4 химические свойства.
H2so4+ h2o. Hno3 h2so4 конц. H2so4 конц + si02. Ph3 h2so4 h2o. Na2so4 химические свойства.
|
 Hno3 h2so4 конц. Hno3 h2so4 конц. Ph3+hno3 разб. Ph3 h2so4 h2o. Ph3 h2so4 h2o.
Hno3 h2so4 конц. Hno3 h2so4 конц. Ph3+hno3 разб. Ph3 h2so4 h2o. Ph3 h2so4 h2o.
|
 Ph3 h2so4 h2o. =. Химические свойства серной кислоты h2so4. So2 h2o h2so3. Mno4- mn+2 - в кислой среде.
Ph3 h2so4 h2o. =. Химические свойства серной кислоты h2so4. So2 h2o h2so3. Mno4- mn+2 - в кислой среде.
|